根據(jù)國家衛(wèi)健委《關(guān)于印發(fā)涉及人的生命科學(xué)和醫(yī)學(xué)研究倫理審查辦法的通知》(國衛(wèi)科教發(fā)〔2023〕4號)精神����,所有涉及人的生物醫(yī)學(xué)研究項目在實施前,需要在國家醫(yī)學(xué)研究登記備案信息系統(tǒng)(以下簡稱備案系統(tǒng),網(wǎng)址:https://www.medicalresearch.org.cn)登記備案�。為此���,廣醫(yī)二院藥物臨床試驗機(jī)構(gòu)從2023年7月1日起�����,將組織在本院開展的符合要求的藥物/醫(yī)療器械臨床試驗項目進(jìn)行備案�����。
一�����、備案范圍:
2023年7月1日后新立項的����,或者在2020年-2023年7月1日期間結(jié)題或仍在進(jìn)行的,且以本院為組長單位及在本院單中心開展的注冊類藥物/醫(yī)療器械臨床試驗���。
二�、注意事項:
熟練掌握“醫(yī)學(xué)研究登記備案信息系統(tǒng)”https://www.medicalresearch.org.cn/login
設(shè)立單位科學(xué)審查委員會���,并在系統(tǒng)備案
設(shè)立單位倫理委員會�,并在系統(tǒng)備案
根據(jù)需要是否需要設(shè)立學(xué)術(shù)委員會(研究者發(fā)起的臨床研究非必需�����,但是臨床藥物實驗�����、干細(xì)胞/體細(xì)胞備案均需要)
三、備案流程:
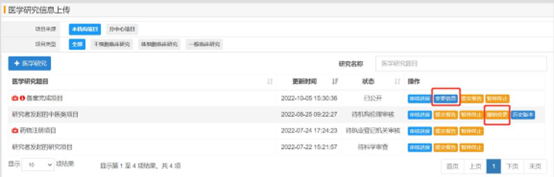
醫(yī)學(xué)研究信息填寫
項目負(fù)責(zé)人新增研究項目或編輯研究項目時����,需要依次填寫項目的各項信息;
![]()
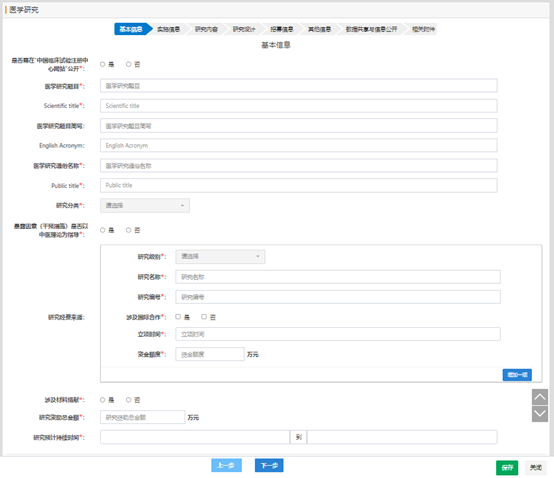
如果有發(fā)文的需求����,需要將項目信息同步到中國臨床試驗注冊中心時, 是否需在“中國臨床試驗注冊中心網(wǎng)站”公開的選項選“是”�,填寫各項需要的英文信息,后續(xù)備案完成后�,會將項目信息同步至中國臨床試驗注冊中心;如果英文信息填寫不對��,或英文信息中填寫中文信息�����,都將不會同步����。
“暴露因素(干預(yù)措施)是否以中醫(yī)理論為指導(dǎo)”選“是”時����,默認(rèn)為中醫(yī)類項目����,提交審核時�,試點省份(目前十二個試點省份(第一批試點省份:北京、上海���、廣州���、海南;第二批試點省份: 河北�、 遼寧、 江蘇���、浙江��、 山東���、 湖南、 重慶��、 四川))需要進(jìn)行學(xué)術(shù)審核�。
實施單位默認(rèn)為項目負(fù)責(zé)人所在的單位�,如果項目負(fù)責(zé)人在其他機(jī)構(gòu)開展的臨床研究���,可以根據(jù)情況變更項目的實施單位��。
對于多中心項目備案時�����,臨床研究分中心選擇“有” �,參與單位可以添加多個���,輸入機(jī)構(gòu)名稱或項目負(fù)責(zé)人時�,會有自動提示�����,有名稱匹配的盡量通過下拉選擇�����,這樣分中心及分中心負(fù)責(zé)人����,登錄后會直接查看到項目;如果手動輸入�����,則匹配不到信息��,分中心及分中心負(fù)責(zé)人看不到該項目的信息���。
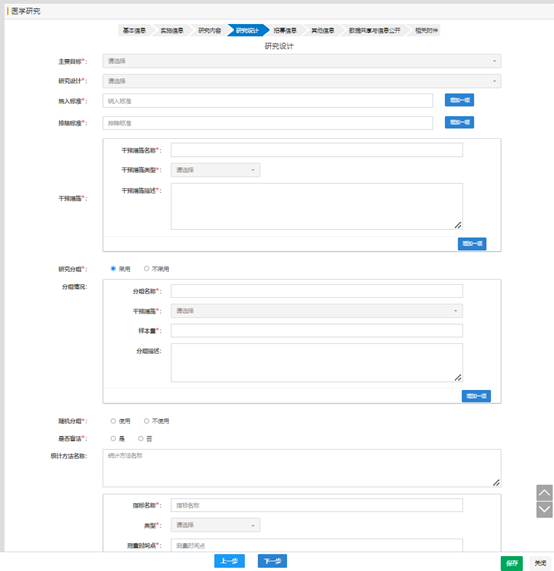
對于干預(yù)性研究�,需要填寫研究自評價的信息����。
項目的學(xué)科分類和 ICD11 分類,請根據(jù)研究項目的所主要治療或觀察的相關(guān)疾病信息���,進(jìn)行選擇���。
研究的具體疾病或癥狀,不用填寫太多無關(guān)的信息�����,只要填寫相關(guān)的疾病名稱或癥狀信息即可。
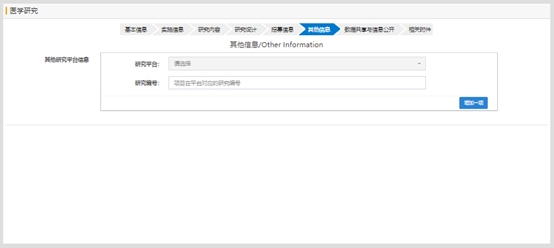
當(dāng)“研究分組”選擇有時���, 分組中的干預(yù)措施需要選擇��,否則提交時會有錯誤提示信息�。
研究項目的招募信息填寫:
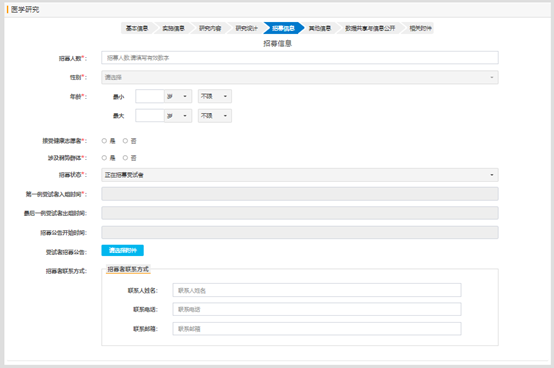
研究項目如果在其他平臺進(jìn)行注冊過�,需要選擇平臺并填寫對應(yīng)平臺的研究編號;如果沒有��,則不需要填寫��;如果選擇了平臺�,不填寫編號的話,提交時���,會提示信息不齊�����,提交失敗�。
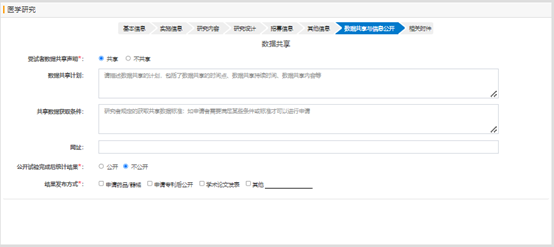
相關(guān)附件部分��,需要上傳研究方案����、知情同意書模板或知情同意豁免申請書�����,
醫(yī)學(xué)研究信息提交
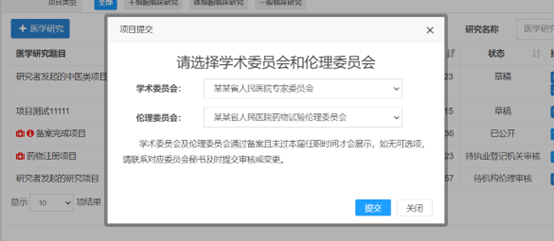
確認(rèn)項目信息填寫無誤后,需要項目負(fù)責(zé)人��,點擊“提交” 按鈕����,提交研究項目審核,授權(quán)人是不能提交審核的�,會出現(xiàn)提交失敗的提示。如果提交時出現(xiàn)信息失敗提示�����,請按照提示信息進(jìn)行補(bǔ)充�����,補(bǔ)充完畢后��,方可提交�����。
研究者提交時,不需要選擇學(xué)術(shù)委員會審核�����,只需要選擇倫理委員會(倫理辦聯(lián)系電話:34153599)進(jìn)行審核����。
常見的提示說明
1、 干預(yù)性研究需要有醫(yī)師
干預(yù)性研究需要項目負(fù)責(zé)人為醫(yī)師�,或者團(tuán)隊成員中有醫(yī)師;如果確認(rèn)團(tuán)隊中有醫(yī)師的話�����,需要在醫(yī)師的個人信息里���,職稱選擇衛(wèi)生技術(shù)人員�,主任醫(yī)師��、副主任醫(yī)師�����、主治醫(yī)師、醫(yī)師��、醫(yī)士中的任一個���,方可提交���。
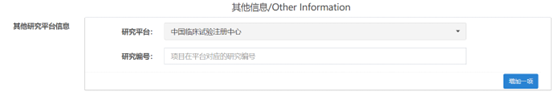
2�、 項目在平臺對應(yīng)的研究編號為空
如果項目在其他信息里選擇了研究平臺的話,就需要填寫對應(yīng)的編號�����,如果不填寫編號進(jìn)行提交的話�����,就會出現(xiàn)上面的提示信息���,如下圖所示:
項目變更
項目信息備案完成后�����,可以進(jìn)行變更���,審核完成的項目進(jìn)行變更時���,將記錄歷史版本信息,方便后續(xù)對比查看���;當(dāng)信息表更后�����,未經(jīng)機(jī)構(gòu)審核前��,可以選擇“撤銷變更”�,還原信息到上一個版本�,如下圖所示